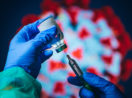
Fiocruz e Butantan pedem uso emergencial de vacinas
Laboratórios pediram autorização à Anvisa para aplicar vacinas da Oxford/Astrazeneca e Coronavac em regime de urgência
07/01/2021
Laboratório Fiocruz, onde está sendo desenvolvida a vacina da Universidade de Oxford e laboratório AstraZeneca / Foto: AE
A Fundação Oswaldo Cruz (Fiocruz) pediu à Agência Nacional de Vigilância Sanitária (Anvisa) o aval para o uso emergencial de 2 milhões de doses da vacina contra a covid-19 desenvolvida pela Universidade de Oxford e a farmacêutica AstraZeneca.
O imunizante é a principal aposta do governo federal para controlar a pandemia. O pedido foi encaminhado nesta sexta-feira, 8 de janeiro, um dia após o anúncio pelo governo de São Paulo da eficácia da vacina Coronavac, que está sendo fabricada pelo Instituto Butantan.
A Anvisa estima um prazo de 10 dias para autorizar ou não o uso emergencial. Esse prazo é interrompido, caso o órgão peça informações dentro do processo.
Mais cedo, o Instituto Butantan pediu a mesma permissão à Anvisa para a Coronavac, vacina desenvolvida pela chinesa Sinovac.
Início da distribuição de vacinas
A Fiocruz deseja distribuir, ainda em janeiro, estas doses prontas, vindas de fábrica indiana.
O produto foi comprado por R$ 59,4 milhões no momento em que o governo federal é pressionado para antecipar o calendário de vacinação no Brasil.
O ministro da Saúde, Eduardo Pazuello, aponta o dia 20 deste mês como data mais otimista para começar a aplicar as doses no País. A imunização com esta vacina exige a aplicação de duas doses.
A Fiocruz também receberá em janeiro insumo farmacêutico para completar a fabricação de cerca de 100 milhões de imunizantes deste modelo.
A ideia é que as primeiras unidades sejam liberadas em fevereiro. No segundo semestre, a Fiocruz afirma que irá realizar todo o processo de fabricação de outras 110 milhões de unidades.
“As primeiras 24h serão utilizadas para fazer uma triagem do processo e checar se os documentos necessários estão disponíveis. Se houver informação importante faltando, a Anvisa pode solicitar as informações adicionais ao laboratório. O prazo de 10 dias não considera o tempo do processo em status de exigência técnica”, disse a Anvisa.
O governo investiu cerca de R$ 2 bilhões para a compra de doses e transferência de tecnologia para a Fiocruz. No plano nacional de imunização, o governo prevê aplicar doses desta vacina em cerca de 50 milhões de brasileiros de grupos prioritários ainda no primeiro semestre.
O governo considera que uma vantagem da vacina de Oxford/AstraZeneca é a facilidade de armazenamento, que exige temperaturas de 2 a 8 graus. Trata-se do intervalo já utilizado na rede de frios do SUS.
A falta de transparência sobre os dados desta vacina, porém, gerou críticas na comunidade científica. Um erro de dosagem levou a dois resultados de eficácia do produto: 62% quando aplicada em um regime de duas doses completas e 90% com meia dose seguida de outra completa. Há ainda dúvidas sobre os resultados para pessoas acima de 55 anos.
Responsável por coordenar o estudo clínico da vacina no Brasil, a médica Lily Yin Weckx disse ao jornal O Estado de S. Paulo que a primeira dose da vacina já mostra eficácia de cerca de 70% contra a doença, mas em intervalo curto. “A gente ainda pode ficar com a média de eficácia de 70%. O estudo continua; teremos um ano de segmento para ver a persistência da proteção, dos anticorpos, de segurança, etc.”
Segundo Lily, “o que é importante é que temos uma vacina segura, eficaz e que pode fazer a diferença na pandemia. Esses número de 60%, 70%, 80% é de proteção contra a doença covid. Mas se considerarmos doenças graves e hospitalização, a vacina foi capaz de evitar quase 100%”.
Ela diz que, entre as pessoas que foram vacinadas, nenhuma teve uma doença grave ou ficou hospitalizada por covid. Todas as hospitalizações ocorreram no grupo controle.
Nova regra facilita compra de vacinas
Uma Medida Provisória assinada pelo presidente Jair Bolsonaro flexibiliza regras para a aquisição de vacinas e insumos farmacêuticos.
Como isso, o Brasil pode comprar insumos e vacinas em fase de desenvolvimento antes mesmo do registro sanitário ou de autorização de uso emergencial pela Agência Nacional de Vigilância Sanitária (Anvisa).
A intenção é tentar dinamizar o processo de aquisição de vacinas, neste momento em que a covid-19 já matou cerca de 200 mil pessoas no Brasil.
A MP foi publicada em edição extra do Diário Oficial da União nesta sexta-feira, 7 de janeiro. A edição extra também traz o despacho do presidente da República que envia o texto para o Congresso Nacional.
A MP flexibiliza normas de licitação, possibilitando que as partes estabeleçam termos contratuais sobre eventual pagamento antecipado.
O texto firma o Plano Nacional de Operacionalização da Vacinação contra a Covid-19 como “instrumento estratégico” de vacinação de toda a população.
A MP também determina que o profissional de saúde esclareça ao paciente ou seu representante legal que o produto não tem registro definitivo na Anvisa, assim como seus riscos e benefícios.
Os estabelecimentos de saúde, públicos e privados, deverão registrar, diariamente e de forma individualizada, os dados referentes à aplicação de vacinas contra a covid-19, assim como de eventuais efeitos colaterais, em um sistema de informação que será disponibilizado pelo Ministério da Saúde.
Pelo texto, a Anvisa poderá conceder autorização excepcional e temporária para a importação e distribuição de quaisquer vacinas contra a covid-19, além de materiais, medicamentos, equipamentos e insumos da área de saúde sujeitos à vigilância sanitária, que não tenham registro na agência desde que esses produtos sejam registrados por, no mínimo, uma autoridade sanitária estrangeira e autorizados à distribuição em seus respectivos países.
Ainda não existem vacinas registradas pela Anvisa. Laboratórios produtores de vacina e seus parceiros no Brasil têm se reunido com a agência reguladora e tratado da documentação necessária para fazer o pedido de uso emergencial da vacina.
Alíquota zero para seringas e agulhas
Uma resolução da Câmara de Comércio Exterior (Camex) concede redução temporária, para zero por cento, da alíquota do Imposto de Importação de seringas e agulhas. A medida tem por objetivo atender as necessidades do Plano Nacional de Operacionalização da Vacinação contra a Covid-19.
O ministro da Saúde, Eduardo Pazuello, em pronunciamento em rede nacional de rádio e TV, na quarta-feira,6, disse que o Brasil tem asseguradas, para este ano, 354 milhões de doses de vacinas contra a covid-19.
Do total, 254 milhões serão produzidas pela Fundação Oswaldo Cruz (Fiocruz), em parceria com a AstraZeneca, e 100 milhões pelo Butantan, em parceria com a empresa Sinovac.
O ministro anunciou também que o ministério está em processo de negociação com os laboratórios Gamaleya, da Rússia, Janssen, Pfizer e Moderna, dos Estados Unidos, e Barat Biotech, da Índia.